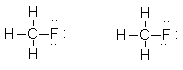Kapitel 10
Lösningarna kan också skrivas ut HÄR| 10.1 | a) Molekyler hos olika gaser har samma medelvärde
på rörelseenergin om de har samma temperatur. b) Rörelse energin ges av formeln W = mv2/2. Ur denna formel kan v som funktion av massan härledas.
Vid en och samma temperatur är W konstant varför √2W = konst och uttrycket kan skrivas
dvs hastigheten är omvänt proportionell mot roten ur molekylens massa, ju större massa desto långsammare rör den sig. Vattenmolekylens massa är 18u medan syremolekylens är 32u. Svar: Vattenmolekylen har högre medelhastighet än syremolekylen. |
|||||||||
| 10.2 | Teori se uppgift 10.1. Molekylmassorna för de tre gaserna är
Svar: medelhastigheten ökar i ordningen SO2 < CO2 < O2 Se även http://www.liber.se/mnt/kemi/Index/ |
|||||||||
| 10.3 | Bindningen mellan kol och klor är polär med negativa
laddning mot kloratomen. Bindningen mellan väte och kol är däremot
icke polär på grund av att elektronegativiteten hos dessa två atomer
är ungefär densamma. De molekyler som uppgiften gäller kan härledas från metan. Molekylernas utseende är en tetraeder med kolatomen i tetraederns tyngdpunkt och de övriga atomerna i dess hörn. Villkoret för att en molekyl är en dipol är att den negativa och positiva tyngdpunkten inte sammanfaller. Molekylerna i b), c) och d) är dipoler. |
|||||||||
| 10.4 | Dipol-dipolbindning är något som kan förekomma mellan
polära molekyler. Den enda som uppfyller detta villkor är
HBr. För de övriga gäller att a) innehåller jonbindning,
b) och c) innehåller kovalenta bindningar utan polärt inslag
och i e) metallbindning. Mellan molekylerna i b) och c) finns van
der Waalsbindning. Se http://www.liber.se/mnt/kemi/Index/ |
|||||||||
| 10.5 | Mellan syremolekylerna och mellan xenonatomerna i fast tillstånd
förekommer van der Waalskrafter. För de övriga gäller
att mellan vattenmolekylerna i fast tillstånd råder vätebindningar
och i natrium- och kalciumoxid är det jonbindningar. |
|||||||||
| 10.6 | Vätebindning uppkommer mellan en väteatom som är
bunden till ett stark eletronegativt element (F, O och N) och ett
annat starkt elektronegativt element med fritt elektronpar. I H2O2
och N2H4 är detta uppfyllt se fig. I uppgift f) och h) kanske du tycker att en vätebindning skulle
vara möjlig, men här är väteatomerna bundna till
kolatomen vilken inte är tillräckligt starkt elektronegativ
och därför kan ingen vätebindning uppkomma.
I uppgift f) och h) kanske du tycker att en vätebindning skulle
vara möjlig, men här är väteatomerna bundna till
kolatomen vilken inte är tillräckligt starkt elektronegativ
och därför kan ingen vätebindning uppkomma.
För övriga gäller att väteatomen inte är bunden till ett tillräckligt elektronegativ element. |
|||||||||
| 10.7 |
I övrigt se lärobokens svar och anvisningar Se även http://www.liber.se/mnt/kemi/Index/ |
|||||||||
| 10.8 | De rätta alternativen är b), d) och e).
I fråga a) och c) är bindningen mellan molekylerna van
der Waals bindning. Varför det inte är vätebindning
se uppgift 10.6 |
|||||||||
| 10.9 | Se lärobokens svar och anvisningar. Jämför med anvisningar till uppgift 10.7 |
|||||||||
| 10.10 | Se lärobokens svar och anvisningar. |
2004 Nationellt centrum för flexibelt lärande