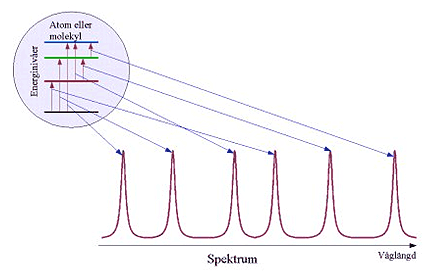
Spektroskopiska analysmetoder
- Energin i atomer och molekyler kan bara anta vissa väl bestämda nivåer. Energin är kvantiserad. Bilden till höger visar energinivåer i väteatomen.
- Elektromagnetisk strålning består av partiklar, små vågpaket, som kallas fotoner.
- Fotonen har en viss energi, som ges av ekvationen
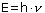
där E är energin, h är Plancks konstant och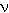 är fotonens frekvens.
är fotonens frekvens.
I synligt ljus beror ljuset färg på dess frekvens. - Kemiska ämnen ger spektra när de växelverkar med elektromagnetisk strålning.
- Många kemiska analysmetoder bygger på att ämnena ger spektra när de utsätts för elektromagnetisk strålning.
Bakgrund
Ett diagram som visar vilka våglängder ett prov sänder ut eller absorberar.
Absorption
Om en atom eller molekyl träffas av en foton kan atomen eller molekylen ta upp energin som finns i fotonen. Fotonen absorberas och försvinner. Detta inträffar dock bara om energin i fotonen precis motsvarar skillnaden mellan två energinivåer i atomen/molekylen. Annars passerar fotonen opåverkad. Strålningen går då rakt genom materian.Emission
En atom/molekyl som tagit upp energi och hamnat i en högre energinivå är exciterad. Den strävar efter att falla tillbaka till lägsta möjliga energinivå. Ett sätt den kan göra detta är genom att avge överskottsenergin i form av en foton. Atomen/molekylen avger elektromagnetisk strålning, t.ex. synligt ljus. Fotonen får då en energi som precis motsvarar skillnaden mellan energinivåerna i atomen/molekylen. Detta är en process som kallas emission. Om exciteringen beror på absorption av strålning kallas processen fluorescens.Ett spektrum kan tala om vilket ämne man har i ett prov.
Energinivåerna i atomer och molekyler är unika för ett visst ämne. Ämnet kommer bara att absorbera strålning där fotonerna har precis de energier som motsvarar skillnaden mellan olika energinivåer. Om man undersöker vilka våglängder som försvinner, när man belyser ämnet med strålning av olika våglängd, får man ett spektrum. Detta kan t.ex. användas för att ta reda på vilket ämne det är.Fundera över
Hur många toppar kommer det att bli i ett spektrum från atomen/molekylen i animeringen här ovan?Analysmetoder
Spektrofotometri
Man kan bestämma ett ämnes koncentration genom att mäta hur mycket ljus ett prov absorberar. Hur mycket strålning som absorberas beror på koncentrationen av det absorberande ämnet. Vi skall titta på hur man kan använda synligt ljus, för att bestämma koncentrationen av ett ämne i en lösning.En apparat som mäter hur mycket ljus ett prov absorberas kallas fotometer. Om man dessutom systematiskt kan variera våglängden, så att man kan få ett spektrum från provet, kallas apparaten en spektrofotometer.
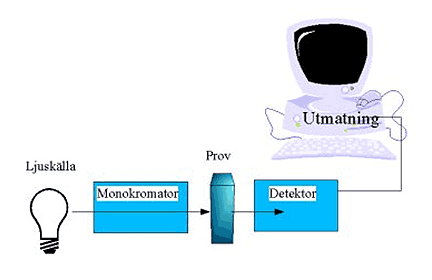
I spektrofotometern mäts hur mycket ljus som skickas in i provet, och hur mycket som passerar genom. Andra spektroskopiska metoderEtt spektrum kan ge information om hur en molekyl ser ut.Energinivåerna i en molekyl påverkas av hur atomerna i molekylen sitter kopplade till varandra. Därför innehåller olika typer av spektra information om den kemiska strukturen hos en molekyl. IR-spektra , kan bland annat tala om vilka funktionella grupper som finns i en molekyl. |
 Spektrofotometer |
Kärnmagnetisk resonans, NMR kan ge information om uppbyggnad, tredimensionell struktur och rörelse hos molekyler.
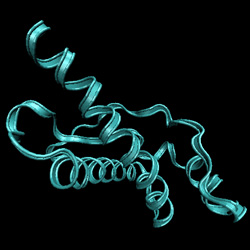
Här till höger ser vi den tredimensionella strukturen hos ett prion-protein. Prioner orsakar bland annat galna ko-sjukan. Bilden visar schematiskt hur peptidkedjan är veckad. Strukturen har bestämts med hjälp av NMR-spektroskopi. |
 |
|