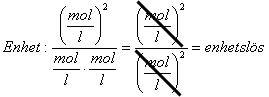Kemisk jämviktsreaktion
|
|
|
Reaktionen mellan vätgas och jodVätgas och jod reagerar gärna med varandra och bildar vätejodid. För att det skall bildas vätejodid måste det finnas både vätgas och jod. |
||
Reaktionen är reversibel, d.v.s. den kan även gå i den andra riktningen. Vätejodid kan sönderdelas till vätgas och jod. |
||
Båda processerna sker parallellt. Väte och jod bildar vätejodid samtidigt som bildad vätejodid sönderfaller till väte och jod. Koncentrationen av de olika ämnena blir konstanta efter en stund, koncentrationerna ges då av massverkans lag. Detta uppstår dock inte i animationen till höger. |
||
Sammanfattningsvis Reaktanter och produkter reagerar hela tiden. En jämvikt ställer in sig mellan reaktanter och produkter. Reaktionen kan skrivas som en jämvikt, med en dubbelriktad reaktionspil. H2 (g) + I2 (g) |
|
Härledning [visa]
Ett exempel på beräkning av jämviktskonstant
Man blandar 0,045 mol H2 med 0,045 mol I2 i en behållare med volymen 1,00 liter vid temperaturen 450 oC. När reaktionen nått jämvikt innehåller behållaren 0,070 mol/l HI. Beräkna jämviktskonstanten för reaktionen
H2 + I2![]() 2 HI
2 HI