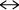- Börja med att skriva upp och balansera reaktionsformeln.
| 2HgO |
 |
2Hg + O2(g) |
- Ta ut de ämnen som är intressanta och placera dessa som
huvuden i en tabell med det ämne man känner något om
till vänster. Koefficienterna skall tas med.
- Överför koefficienterna frĺn den förkortade reaktionsformeln till
tabellen.
- Ange hur stor substansmängd (antal mol) 1 mol av det ämne
vi känner något om (HgO) svarar mot det ämne vi söker
något om.
- Sätt in aktuella värden i tabellen.
| 2HgO |
 |
O2 |
| m (g) |
M (g/mol) |
n (mol) |
n (mol) |
M (g/mol) |
m (g) |
| |
|
2 |
1 |
|
|
| |
|
1 |
½ |
|
|
| 25 |
200,6+16=216,6 |
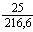 |
=0,115 |
|
½·0115=0,0577 |
16+16=32 |
0,0577· 32=
= 1,85 |
|
Svar: 1,9 g syrgas bildas
Till början av Exempel 1
|